Мир вокруг сложен и разнообразен. Только редкие химические элементы в обычных условиях существуют в состоянии одноатомного газа. В большинстве своем атомы элементов являются составными частями молекул или кристаллических решеток. А из них, в свою очередь, состоит все в этом мире.
Энциклопедический словарь дает определение химической связи как «взаимодействие атомов, обусловливающее их соединение в молекулы и кристаллы». Соответственно, химическая связь – это первопричина удержания атомов друг рядом с другом, образования молекул, кристаллов, веществ.
 Главную роль в химической связи отводят электронам, расположенным на внешней оболочке атомов, наименее прочно связанным с ядром. Иначе такие электроны называются валентными.
Главную роль в химической связи отводят электронам, расположенным на внешней оболочке атомов, наименее прочно связанным с ядром. Иначе такие электроны называются валентными.
Термин «валентность» переводится с латинского языка как «имеющий силу». Это и есть особая сила атома присоединять или замещать некоторое количество других атомов, либо их групп, с образованием химической связи. Цель атомов, с которой они вступают в химическую связь – достижение наиболее устойчивой, имеющей наименьшую энергию, конфигурации. В химии валентность химических элементов встречается постоянная и переменная.
В химии принято выделять разные типы химических связей.
Внутримолекулярные:
- ионная;
- ковалентная;
- металлическая;
Межмолекулярные:
- водородная;
- вандерваальсовая;
- ион-дипольное;
- диполь-дипольное.
 Тип связи зависит напрямую от электроотрицательности участвующих атомов, способности атомов притягивать в соединении к себе электроны. Наименьшими показателями обладают типичные металлы, наибольшими – неметаллы.
Тип связи зависит напрямую от электроотрицательности участвующих атомов, способности атомов притягивать в соединении к себе электроны. Наименьшими показателями обладают типичные металлы, наибольшими – неметаллы.
Ионная связь возникает, если между взаимодействующими атомами есть резкое отличие по электроотрицательности.
Металлическая связь характерна для простых веществ, металлов. Сущность процесса во взаимодействии относительно свободных электронов с ионами металлов.
Водородная связь достаточно специфична. В ней участвуют атомы водорода и атомы сильно электроотрицательного элемента.
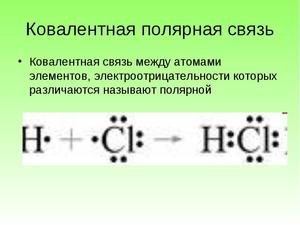
Ковалентная связь подразделяется на полярную и неполярную ковалентные связи. При этом неполярная ковалентная связь образуется при взаимодействии атомов с одинаковой электроотрицательностью, а полярная – в случае, если отличие крайне мало.
 Все данные атомов, молекул, важны не только для расчетов формул и понимания химической связи. Природа реагентов – один из факторов, влияющих на результат и скорость химической реакции с любыми веществами. На основе определения природы имеющихся молекул, можно проводить практические опыты, химические реакции. Однако знание валентности и химической связи помогут в их проведении.
Все данные атомов, молекул, важны не только для расчетов формул и понимания химической связи. Природа реагентов – один из факторов, влияющих на результат и скорость химической реакции с любыми веществами. На основе определения природы имеющихся молекул, можно проводить практические опыты, химические реакции. Однако знание валентности и химической связи помогут в их проведении.
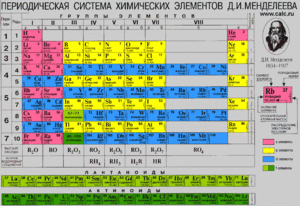
Валентность – одна из основных характеристик химических элементов. Номер группы, обозначенный римской цифрой над вертикальным столбиком в периодической таблице Менделеева, соответствует значению валентности элемента.
Также рекомендую изучить следующие уроки этого раздела:




 ноября 26, 2018
ноября 26, 2018  Светлана Козлова
Светлана Козлова  Опубликовано в рубрике
Опубликовано в рубрике  Метки:
Метки: 